DJ Bayer bekommt EU-Empfehlung für 6-Monats-Behandlungsintervall mit Eylea 8mg
DOW JONES--Bayer hat vom Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittel-Agentur für sein Augenmedikament Eylea 8mg die Empfehlung für eine Verlängerung der Behandlungsintervalle von zwei Netzhauterkrankungen auf bis zu sechs Monate bekommen. Eine Entscheidung der EU-Kommission werde in den nächsten Wochen erwartet, teilte Bayer in Berlin mit. Hochdosiertes Eylea hätte damit ein Alleinstellungsmerkmal bei der Behandlung der feuchten altersabhängigen Makuladegeneration (nAMD) und dem diabetischen Makulaödem (DMÖ) in Europa.
Bislang gilt eine Zulassung für bis zu 5-monatige Behandlungsintervalle. Da das Medikament in den Augapfel gespritzt werden muss, ist ein längeres Behandlungsintervall für Patienten von großem Nutzen.
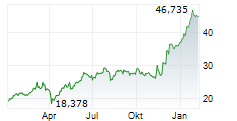
Bayer hat 2024 mit Eylea einen Umsatz von 3,3 Milliarden Euro erzielt. Der Patentschutz des Wirkstoffs Aflibercept läuft im November aus. Bayer verfügt jedoch über Patente für höherdosierte Formulierungen in verschiedenen Anwendungen.
Die verlängerten Intervalle, kombiniert mit dem einzigartigen Produktprofil von Eylea 8 mg hätten das Potential ein neuer Standard in der Behandlung von Netzhauterkrankungen zu werden, sagte Christine Roth, die Leiterin für Global Product Strategy and Commercialization bei Bayer.
Kontakt zum Autor: olaf.ridder@wsj.com
DJG/rio/kla
(END) Dow Jones Newswires
May 23, 2025 02:56 ET (06:56 GMT)
Copyright (c) 2025 Dow Jones & Company, Inc.