DJ Novo Nordisk beantragt US-Zulassung für Abnehm-Medikament CagriSema
Von Dominic Chopping
DOW JONES--Novo Nordisk hat bei der US-Gesundheitsbehörde FDA die Zulassung für CagriSema beantragt. Das ist eine einmal wöchentlich zu verabreichende Spritze, die zwei Wirkstoffe zur Behandlung von Fettleibigkeit kombiniert.
CagriSema kombiniert den Hauptbestandteil von Wegovy mit Cagrilintid, einem experimentellen Wirkstoff, der ein Hormon namens Amylin nachahmt, welches den Appetit reguliert.
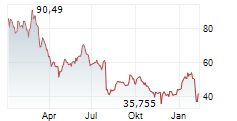
Frühe Studiendaten zu CagriSema hatten Ende vergangenen Jahres die Anleger mit dem erzielten Gewichtsverlust enttäuscht und fast 100 Milliarden US-Dollar an Börsenwert des Arzneimittelherstellers vernichtet. Die Studie zeigte, dass übergewichtige oder fettleibige Freiwillige ohne Typ-2-Diabetes nach 68 Wochen durchschnittlich 22,7 Prozent ihres Gewichts verloren, was unter den von Novo Nordisk erwarteten 25 Prozent lag.
Der dänische Pharmakonzern teilte am Donnerstag mit, dass CagriSema im Falle einer Zulassung Patienten und medizinischem Fachpersonal eine zusätzliche Behandlungsoption bieten würde, um den ungedeckten medizinischen Bedarf bei Fettleibigkeit zu decken und das langfristige Krankheitsmanagement zu unterstützen.
"CagriSema hat das Potenzial, einen bedeutenden Schritt nach vorn in der ganzheitlichen Behandlung von Fettleibigkeit darzustellen", sagte CEO Mike Doustdar. Das Sicherheitsprofil sei vergleichbar mit Medikamenten wie Wegovy.
Es wird erwartet, dass die FDA den Antrag für CagriSema im Jahr 2026 prüft.
Novo Nordisk wartet derzeit noch auf die FDA-Zulassung für seine Wegovy-Abnehmpille, mit der das Unternehmen noch vor Jahresende rechnet.
Kontakt zum Autor: unternehmen.de@dowjones.com
DJG/DJN/mgo/kla
(END) Dow Jones Newswires
December 18, 2025 09:08 ET (14:08 GMT)
Copyright (c) 2025 Dow Jones & Company, Inc.