DJ FDA verwarnt Novo wegen nicht gemeldeter Nebenwirkungen bei GLP-1-Mitteln
Von Elias Schisgall
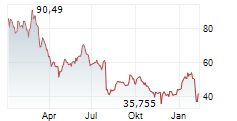
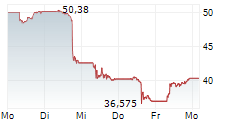
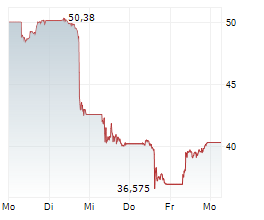
DOW JONES--Novo Nordisk hat von der US-Arzneimittelbehörde FDA eine Verwarnung erhalten. Der Pharmakonzern hat es versäumt, schwerwiegende vermutete Nebenwirkungen seiner GLP-1-Präparate zu melden.
In einem Brief vom Donnerstag betonte die FDA mehrere Fälle, darunter zwei Todesfälle und einen Suizid im Zusammenhang mit Patienten, die Semaglutid einnahmen - den Wirkstoff, den Novo in seinen Medikamenten Ozempic bzw. Wegovy vermarket.
Die Arzneimittelbhörde erklärte, Novo Nordisk habe einen Fall zu Unrecht für unbegründet erklärt und die beiden anderen Fälle nicht an die FDA gemeldet. Sie kam zu keinem Schluss darüber, ob die Todesfälle mit dem GLP-1-Medikament in Zusammenhang standen.
Die Richtlinien des Konzerns bezüglich der Meldung vermuteter Nebenwirkungen stimmten mit den FDA-Vorschriften überein, hieß es. Andere unerwünschte Ereignisse seien zu Unrecht für nichtig erklärt oder nicht innerhalb der vorgeschriebenen Frist von 15 Tagen an die FDA übermittelt worden.
Die Erkenntnisse der FDA basieren auf einer Inspektion einer Novo-Einrichtung, die Anfang 2025 durchgeführt wurde. Die Behörde würdigte die Korrektur- und Vorbeugungsmaßnahmen von Novo seit der Inspektion, sagte jedoch, dass die Antworten des Unternehmens nicht sicherstellten, dass künftige Verstöße verhindert würden. Sie gab dem Konzern 15 Tage Zeit, um sie über Maßnahmen zu informieren, die ergriffen werden, um künftige Verstöße zu verhindern.
Novo Nordisk erklärte, man arbeite zügig daran, auf die Anfrage der FDA zu reagieren. Das Unternehmen habe regelmäßig mit der Behörde über seinen Plan für Korrektur- und Vorbeugungsmaßnahmen kommuniziert. Der nun verschickte Brief lasse keine Rückschlüsse auf die Qualität oder Sicherheit seiner Therapien zu.
Kontakt zum Autor: unternehmen.de@dowjones.com
DJG/DJN/sha/ros
(END) Dow Jones Newswires
March 10, 2026 12:30 ET (16:30 GMT)
Copyright (c) 2026 Dow Jones & Company, Inc.