| Realtime | Geld | Brief | Zeit |
|---|---|---|---|
| 19,240 | 19,320 | 19:16 | |
| 19,260 | 19,340 | 19:16 |
- Alle
- Pressemitteilungen
- Empfehlungen
- Chartanalysen
- Berichte
| Zeit | Aktuelle Nachrichten Sprache:
Alle DE EN | Leser | Medien | ||
|---|---|---|---|---|---|
| 05.05. | Santhera Pharmaceuticals Holding AG: Santhera Publishes Agenda for its Annual General Meeting | 337 | GlobeNewswire (Europe) | Ad hoc announcement pursuant to Art. 53 LR.
Pratteln, Switzerland, May 5, 2026 - Santhera Pharmaceuticals (SIX: SANN) today published the invitation to its Annual General Meeting (AGM), which will... ► Artikel lesen | |
| 05.05. | Santhera Pharmaceuticals Holding AG: Santhera veröffentlicht Einladung zur ordentlichen Generalversammlung | 542 | GlobeNewswire (Deutschland) | Ad-hoc-Mitteilung gemäss Art. 53 KR.
Pratteln, Schweiz, 5. Mai 2026 - Santhera Pharmaceuticals (SIX: SANN) hat heute die Einladung zur ordentlichen Generalversammlung (GV) veröffentlicht, die am... ► Artikel lesen | |
| 30.04. | Santhera nominiert Ex-Idorsia-Chefin Srishti Gupta als Verwaltungsratsmitglied | 468 | Moneycab | Pratteln - Santhera schlägt der bevorstehenden Generalversammlung am 26. Mai die Wahl von Srishti Gupta in den Verwaltungsrat vor. Diese war von Juli 2025 bis Mitte März 2026 die Chefin von Idorsia.... ► Artikel lesen | |
| 30.04. | Santhera Pharmaceuticals Holding AG: Santhera Proposes Dr. Srishti Gupta as New Member of the Board of Directors | 330 | GlobeNewswire (Europe) | Ad hoc announcement pursuant to Art. 53 LR.
Pratteln, Switzerland, April 30, 2026 - Santhera Pharmaceuticals (SIX: SANN) proposes to elect Dr. Srishti Gupta, MD, MPP, MPhil, as an Independent Director... ► Artikel lesen | |
| 30.04. | Santhera Pharmaceuticals Holding AG: Santhera schlägt Dr. Srishti Gupta als neues Mitglied des Verwaltungsrats | 463 | GlobeNewswire (Deutschland) | Ad-hoc-Mitteilung gemäss Art. 53 KR.
Pratteln, Schweiz, 30. April 2026 - Santhera Pharmaceuticals (SIX: SANN) schlägt vor, Dr. Srishti Gupta, MD, MPP, MPhil, auf der bevorstehenden ordentlichen... ► Artikel lesen | |
| 28.04. | Santhera FY2025 slides: revenue doubles, AGAMREE captures market share | 11 | Investing.com | ||
| SANTHERA PHARMACEUTICALS Aktie jetzt für 0€ handeln | |||||
| 28.04. | Santhera erhält positive Entscheidung aus Italien für Agamree-Rückerstattung | 21 | cash | ||
| 28.04. | Santhera Pharmaceuticals Holding AG: Santhera Pharmaceuticals Full Year Results for the Year Ended 31 December 2025 | 641 | GlobeNewswire (Europe) | Ad hoc announcement pursuant to Art. 53 LR
A conference call will be held on April 28, 2026, at 14:00 CEST / 13:00 BST / 08:00 EDT. Details are at the end of this news release
AGAMREE delivers... ► Artikel lesen | |
| 28.04. | Santhera Pharmaceuticals Holding AG: Santhera gibt positive Entscheidung des AIFA-Vorstands zur Erstattung von AGAMREE (Vamorolon) in Italien bekannt | 468 | GlobeNewswire (Deutschland) | Pratteln, Schweiz, 28. April 2026 - Santhera Pharmaceuticals (SIX: SANN) gibt bekannt, dass der Vorstand der italienischen Arzneimittelbehörde AIFA die Erstattung von AGAMREE (Vamorolon) für die Behandlung... ► Artikel lesen | |
| 28.04. | Santhera Pharmaceuticals Holding AG: Santhera Announces Positive AIFA Board Decision on Reimbursement of AGAMREE (vamorolone) in Italy | 357 | GlobeNewswire (Europe) | Pratteln, Switzerland, April 28, 2026 - Santhera Pharmaceuticals (SIX: SANN) announces that the Board of Directors of the Italian Medicines Agency, AIFA, has approved the reimbursement of AGAMREE (vamorolone)... ► Artikel lesen | |
| 28.04. | Santhera Pharmaceuticals Holding AG: Santhera Pharmaceuticals Jahresergebnisse für das am 31. Dezember 2025 endende Geschäftsjahr | 514 | GlobeNewswire (Deutschland) | Ad-hoc-Mitteilung gemäss Art. 53 KR.
Am 28. April 2026 findet um 14:00 Uhr MESZ / 13:00 Uhr BST / 08:00 Uhr EDT eine Telefonkonferenz statt. Einzelheiten finden Sie am Ende dieser Pressemitteilung
AGAMREE... ► Artikel lesen | |
| 27.04. | Santhera Pharmaceuticals Holding AG: Santhera Receives Positive CHMP Opinion to Expand AGAMREE (vamorolone) Use in Pediatric DMD Patients Aged Two and Older in the EU | 386 | GlobeNewswire (Europe) | Pratteln, Switzerland, April 27, 2026 - Santhera Pharmaceuticals (SIX: SANN) today announced that the Committee for Medicinal Products for Human Use (CHMP) of the European Medicines Agency (EMA) has... ► Artikel lesen | |
| 27.04. | Santhera Pharmaceuticals Holding AG: Santhera erhält positive Stellungnahme des CHMP zur Ausweitung der Anwendung von AGAMREE (Vamorolon) bei pädiatrischen DMD-Patienten ab zwei Jahren in der EU | 516 | GlobeNewswire (Deutschland) | Pratteln, Schweiz, 27. April 2026 - Santhera Pharmaceuticals (SIX: SANN) gab heute bekannt, dass der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittelagentur (EMA) eine positive Stellungnahme... ► Artikel lesen | |
| 23.04. | Santhera ernennt Orlando Oliveira zum neuen CEO nach Rücktritt von Eklund | 381 | Moneycab | Pratteln - Bei Santhera kommt es zu einem Wechsel an der Spitze: Konzernchef Dario Eklund tritt nach knapp 7 Jahren zurück. Zu seinem Nachfolger wurde Orlando Oliveira ernannt, der sein Amt am 15. Juli... ► Artikel lesen | |
| 23.04. | Santhera Pharmaceuticals Holding AG: Santhera Appoints Orlando Oliveira as Chief Executive Officer | 387 | GlobeNewswire (Europe) | Ad hoc announcement pursuant to Art. 53 LR.
Dario Eklund to hand over leadership following planned transition
Pratteln, Switzerland, April 23, 2026 - Santhera Pharmaceuticals (SIX: SANN) announces... ► Artikel lesen | |
| 23.04. | Santhera Pharmaceuticals Holding AG: Santhera ernennt Orlando Oliveira zum Chief Executive Officer | 547 | GlobeNewswire (Deutschland) | Ad-hoc-Mitteilung gemäss Art. 53 KR.
Dario Eklund übergibt die leitung nach geplanter übergangsphase
Pratteln, Schweiz, 23. April 2026 - Santhera Pharmaceuticals (SIX: SANN) gibt die Ernennung... ► Artikel lesen | |
| 12.03. | Santhera Pharmaceuticals Holding AG: Full Year 2025 Trading Update | 647 | GlobeNewswire (Europe) | Ad hoc announcement pursuant to Art. 53 LR
AGAMREE continues to build strong commercial momentum, delivering 98% revenue growth
Pratteln, Switzerland, March 12, 2026 - Santhera Pharmaceuticals... ► Artikel lesen | |
| 12.03. | Santhera Pharmaceuticals Holding AG: Handelsupdate für das Geschäftsjahr 2025 | 758 | GlobeNewswire (Deutschland) | Ad-hoc-Mitteilung gemäss Art. 53 KR
AGAMREE setzt starke Geschäftsentwicklung fort und erzielt Umsatzwachstum von 98%
Pratteln, Schweiz, 12. März 2026 - Santhera Pharmaceuticals (SIX: SANN)... ► Artikel lesen | |
| 11.03. | Skyhawk taps Teva alum to steer commercial path, while Santhera names new CCO to grow DMD sales | 38 | FiercePharma | ||
| 10.03. | Santhera Pharma Appoints Marc Clausse As Chief Commercial Officer | 12 | RTTNews |
1 2 3 4 Weiter >>
65 Nachrichten in den letzten 12 Monaten
| Unternehmen / Aktien | Aktienkurs | % | Top-Nachrichten | ||
|---|---|---|---|---|---|
| BAYER | 37,970 | -1,22 % | Bayer stärkt Pipeline potentieller Augenmedikamente mit Übernahme | BERLIN/SAN FRANCISCO (dpa-AFX) - Bayer will sein Geschäft mit Augenmedikamenten mit einer Übernahme in den USA stärken. Mit der Akquisition von Perfuse Therapeutics erhält der Pharmakonzern laut einer... ► Artikel lesen | |
| NOVO NORDISK | 40,105 | +0,12 % | Starker Marktstart für neue Abnehmpille: Novo Nordisk wird optimistischer | BAGSVAERD (dpa-AFX) - Der dänische Pharmahersteller Novo Nordisk hebt nach einem überraschend schwungvollen ersten Quartal seine Ziele für das Gesamtjahr leicht an. Grund seien die inzwischen aufgehellten... ► Artikel lesen | |
| PFIZER | 22,025 | -0,11 % | JEFFERIES stuft PFIZER INC auf 'Buy' | NEW YORK (dpa-AFX Analyser) - Das Analysehaus Jefferies hat Pfizer mit einem Kursziel von 35 US-Dollar auf "Buy" belassen. Der Pharmakonzern habe im ersten Quartal positiv überrascht und die Jahresziele... ► Artikel lesen | |
| NOVARTIS | 127,28 | +0,97 % | Warum Biotech-Aktien jetzt im Umbruch sind und Zelltherapie nicht nur bei BioNTech, Morphosys und Co. ein Thema ist. | ||
| MERCK KGAA | 121,15 | +7,21 % | UBS stuft MERCK KGAA auf 'Buy' | ZÜRICH (dpa-AFX Analyser) - Die Schweizer Großbank UBS hat die Einstufung für Merck KGaA vor Zahlen zum ersten Quartal mit einem Kursziel von 150 Euro auf "Buy" belassen. In der Pharmasparte könne ein... ► Artikel lesen | |
| GILEAD SCIENCES | 114,02 | -0,82 % | Gilead: Erwartungen übertroffen - darum fällt die Aktie trotzdem | Die Biotech-Gesellschaft Gilead Sciences hat am Donnerstagabend nach US-Börsenschluss die Zahlen für das erste Quartal des neuen Geschäftsjahres veröffentlicht. Trotz besser als erwarteter Vorgaben... ► Artikel lesen | |
| AURORA CANNABIS | 2,908 | +1,47 % | AURORA CANNABIS INC: Ruhe vor dem nächsten Impuls | ||
| SANOFI | 72,85 | -0,75 % | Mesoblast Aktie: Warum sich der Blick auf diesen Biotech-Player jetzt lohnt - und was Anleger von Merck, Regeneron & Co. lernen können | ||
| GSK | 21,720 | -0,32 % | GSK findet für neues Hepatitis-Medikament Vertriebspartner in China | DJ GSK findet für neues Hepatitis-Medikament Vertriebspartner in China
Von Adria Calatayud
DOW JONES--GSK kooperiert mit Sino Biopharmaceutical, um die Markteinführung für sein Hepatitis-B-Medikament... ► Artikel lesen | |
| ABBVIE | 177,30 | +0,11 % | Ihre wichtigsten Termine: Heute im Fokus: AbbVie, Colgate-Palmolive, Toyota, Sony, Krones, Bechtle, Evonik | © Foto: Hiro Komae/AP/dpaGut geplant in den Tag. Mit dem wO-Tagesausblick haben Sie die wichtigsten Termine im Blick und starten bestens vorbereitet in den neuen Handelstag.Unternehmenstermine 05:00... ► Artikel lesen | |
| ROCHE | 348,85 | -0,13 % | Roche stärkt KI-Diagnostik mit Kauf von PathAI für bis zu 1,05 Mrd USD | DJ Roche stärkt KI-Diagnostik mit Kauf von PathAI für bis zu 1,05 Mrd USD
Von Adria Calatayud
DOW JONES--Roche Holdings übernimmt PathAI für bis zu 1,05 Milliarden US-Dollar, um die auf Künstlicher... ► Artikel lesen | |
| CANOPY GROWTH | 0,940 | +0,92 % | CANOPY GROWTH CORPORATION: Struktur vor Impuls | ||
| STADA ARZNEIMITTEL | - | - | Enzymatica AB: Quarterly report Q1/2026 - Enzymatica strengthens international position through STADA agreement | First quarter
Net sales amounted to SEK 11.4 million (12.3).
Operating result amounted to SEK -13.6.million (-18.0)
Earnings per share, before... ► Artikel lesen | |
| ELI LILLY | 864,00 | +2,45 % | Wegovy treibt die Milliarden: Novo-Aktie haussiert - aber Eli Lilly nimmt dem Konzern gerade den Markt weg | © Foto: Richard Drew - APStarke Quartalszahlen treffen auf brutalen Wettbewerb. Während Novo auf Wegovy setzt, zieht Lilly nach. Für Anleger geht es jetzt um Timing - ist das der Turnaround oder der... ► Artikel lesen | |
| MERCK & CO | 97,27 | +1,62 % | BioInvent International: BioInvent's TNFR2 Antibody BI-1808 Shows Strong Activity and Immune Activation as Single Agent and in Combination with KEYTRUDA in Advanced CTCL | 40% objective response rate (ORR) as single agent in heavily pre-treated patients with advanced Cutaneous T-Cell Lymphoma (CTCL)Durable responses observed, including a complete response lasting over... ► Artikel lesen |
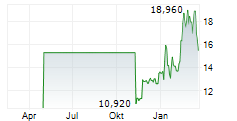
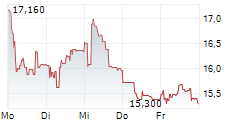
Das Unternehmen SANTHERA PHARMACEUTICALS HOLDING AG kann der Branche Pharma zugeordnet werden. Mit einer aktuellen Kursveränderung von +0,360 (+1,90 %) liegt der Kurs bei 19,260 Euro.
VerkaufenHaltenKaufen
■ Verkaufen
■ Halten
■ Kaufen
Sie erhalten auf FinanzNachrichten.de kostenlose Realtime-Aktienkurse von und sowie Kurse und Daten von ARIVA.DE AG.
Weitere Kennzahlen, Fundamentaldaten und Unternehmensinformationen zu SANTHERA PHARMACEUTICALS HOLDING AG finden Sie auf Wallstreet Online.